HLX71為復宏漢霖自主開發的一款C末端帶有IgG1 Fc的重組人血管緊張素轉換酶2(human Angiotensin converting enzyme 2,hACE2)融合蛋白。新冠病毒感染人體細胞的關鍵步驟之一為病毒表面S蛋白S1亞基的受體結合區(Receptor binding domain,RDB)與人體細胞表面的hACE2蛋白結合,從而引發人體細胞的內吞作用將病毒吞入細胞內[1,2]。HLX71一端的ACE2蛋白可充當「誘餌」,與SARS-CoV-2病毒S蛋白的RBD區域結合,且具有較強的結合力,當HLX71與病毒的RBD區域結合後,可以阻斷病毒與宿主細胞表面的ACE2結合,防止SARS-CoV-2病毒感染細胞,進而用於新冠肺炎的治療。
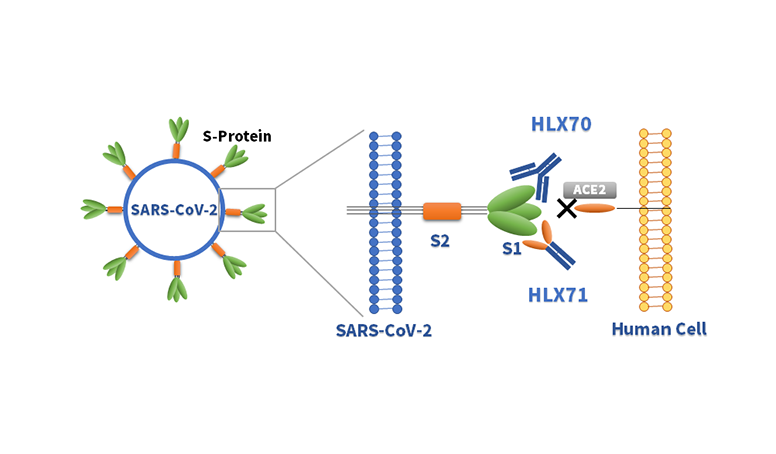
遵從人用藥物註冊技術要求國際協調會議(ICH)的指導原則,復宏漢霖對HLX71進行了藥理學、葯代動力學和毒理學等臨床前研究,以評估HLX71的有效性和安全性。一系列臨床前研究結果表明,HLX71能夠顯著抑制SARS-CoV-2病毒感染,且靜脈注射HLX71具有良好的安全性。另一款由復宏漢霖自主開發的新冠病毒中和抗體HLX70同樣能夠結合到病毒表面的RBD區域,抑制SARS-CoV-2病毒感染。復宏漢霖正探索兩款自有抗新冠候選藥物HLX70和HLX71的協同作用,在已開展的聯合用藥分析中,HLX71與HLX70展現出協同阻斷RBD與細胞表面hACE2結合的能力。在進一步評估HLX70和HLX71的療效及其聯合用藥方案的同時,復宏漢霖也在準備相關候選藥物的臨床試驗,為抗疫貢獻更多力量。
參考文獻
[1] Gallagher T M, Buchmeier M J. Coronavirus spike proteins in viral entry and pathogenesis[J]. Virology, 2001, 279(2): 371-374.
[2] Yan R, Zhang Y, Li Y, et al. Structural basis for the recognition of SARS-CoV-2 by full-length human ACE2[J]. Science, 2020, 367(6485): 1444-1448.
