5月21日,復宏漢霖聯合創始人、首席執行官劉世高博士應邀參加了由Cytiva(思拓凡)舉辦的「創新應變,『生』生不息」線上生物醫藥發展趨勢研討會,並在研討會上發表了主題演講-「中國生物葯開發之路和新一代生產技術的應用」,向與會嘉賓介紹了復宏漢霖在一次性生產技術、連續流生產技術等創新技術開發與應用方面的成功經驗和最新進展。

復宏漢霖聯合創始人、首席執行官 劉世高 博士
生產技術的不斷優化與創新是保證生物葯質高價優、更可負擔的關鍵所在,也是中國生物醫藥行業能夠快速發展不可或缺的引擎。復宏漢霖自成立之初即結合自身發展需求,持續探索國際前沿生物葯生產技術的應用,並積極與業界分享經驗,致力於帶動國內生物葯生產技術的不斷進步。
劉世高博士首先對中國生物葯發展現狀進行了概括性的綜述,認為中國生物醫藥產業將在近年來迎來巨大的發展機遇。在全球生物葯增長勢頭強勁,中國巨大的醫療需求亟需滿足的大環境下,中國生物葯市場預期能夠迎來迅猛增長。其中,生物類似葯市場份額的佔比將持續提升。中國首個生物類似葯漢利康(利妥昔單抗注射液)由復宏漢霖自主開發,於2019年2月獲得國家藥品監督管理局的批准,開啟了中國生物類似葯的新時代。復宏漢霖另外一款重磅生物類似葯HLX02(注射用曲妥珠單抗)的國際化布局成果也已凸顯,是中國首個在本土開發生產並在歐盟申報上市的單抗生物類似葯,也是首個獲得歐盟GMP批准的「中國籍」曲妥珠單抗。
劉世高博士首先對中國生物葯發展現狀進行了概括性的綜述,認為中國生物醫藥產業將在近年來迎來巨大的發展機遇。在全球生物葯增長勢頭強勁,中國巨大的醫療需求亟需滿足的大環境下,中國生物葯市場預期能夠迎來迅猛增長。其中,生物類似葯市場份額的佔比將持續提升。中國首個生物類似葯漢利康(利妥昔單抗注射液)由復宏漢霖自主開發,於2019年2月獲得國家藥品監督管理局的批准,開啟了中國生物類似葯的新時代。復宏漢霖另外一款重磅生物類似葯HLX02(注射用曲妥珠單抗)的國際化布局成果也已凸顯,是中國首個在本土開發生產並在歐盟申報上市的單抗生物類似葯,也是首個獲得歐盟GMP批准的「中國籍」曲妥珠單抗。
無論是生物類似葯還是創新葯的生產,復宏漢霖都始終堅持嚴格遵守國際和中國的質量標準,在此條件下積極開展創新型生產技術的研發與產業化探索,在實現生物葯生產流程的自動化、信息化與智能化的道路上始終處於行業領跑者的地位。復宏漢霖在中國率先應用一次性生產技術,近年來,公司更是積極推動連續流生產技術的研發,已順利完成實驗室級別和中試級別(200L)連續流生產技術的概念測試。
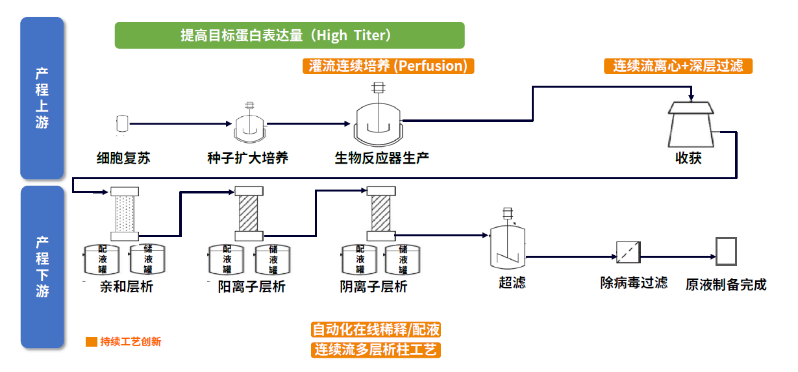
連續流生產技術開發中的持續工藝創新
連續流生產是生物葯生產技術發展的大勢所趨,能夠提高生產過程的穩健性和可靠性、降低生產和固定資產支出、減少工廠建造時間、降低生產中產品更換所需時間。連續流生產在上游生產中主要通過灌流細胞培養工藝來實現。近年來,切向流過濾技術(TFF)與交替切向流過濾技術(ATF)的逐漸完善使得上游灌流細胞培養過程中細胞密度得以大幅提升,從而實現抗體生產滴度的顯著增加。復宏漢霖實驗數據顯示,灌流細胞培養中單個1000L一次性生物反應器的抗體生產滴度可達40g/L,抗體年產量可超過150kg;而補料批次培養(fed-batch)條件下,1個2000L一次性生物反應器的抗體生產滴度約為5g/L,受滴度限制,年產量約為100kg。
在下游生產過程中,連續流的實現主要通過採用連續流層析、在線檢測等技術將多個工藝單元進行整合,可以在提高生產效率與廠房利用率的同時,減小中間體存儲量、各步驟之間的等待時間以及儀器設備所需的規模和對應的投入,從而達到縮短生產周期與降低生產成本的目標。復宏漢霖在下游連續生產實驗室規模概念測試中,實現了7步抗體純化步驟的連結整合和自動運行,可將下游處理速度提升4-5倍,且產品質量穩定;200L中試規模連續流概念測試亦於近期取得成功,下游生產周期可縮短至1.5天左右,純化回收率與傳統的批次模式基本相當且產品質量穩定,質量數據具有良好的可重複性。
在下游生產過程中,連續流的實現主要通過採用連續流層析、在線檢測等技術將多個工藝單元進行整合,可以在提高生產效率與廠房利用率的同時,減小中間體存儲量、各步驟之間的等待時間以及儀器設備所需的規模和對應的投入,從而達到縮短生產周期與降低生產成本的目標。復宏漢霖在下游連續生產實驗室規模概念測試中,實現了7步抗體純化步驟的連結整合和自動運行,可將下游處理速度提升4-5倍,且產品質量穩定;200L中試規模連續流概念測試亦於近期取得成功,下游生產周期可縮短至1.5天左右,純化回收率與傳統的批次模式基本相當且產品質量穩定,質量數據具有良好的可重複性。
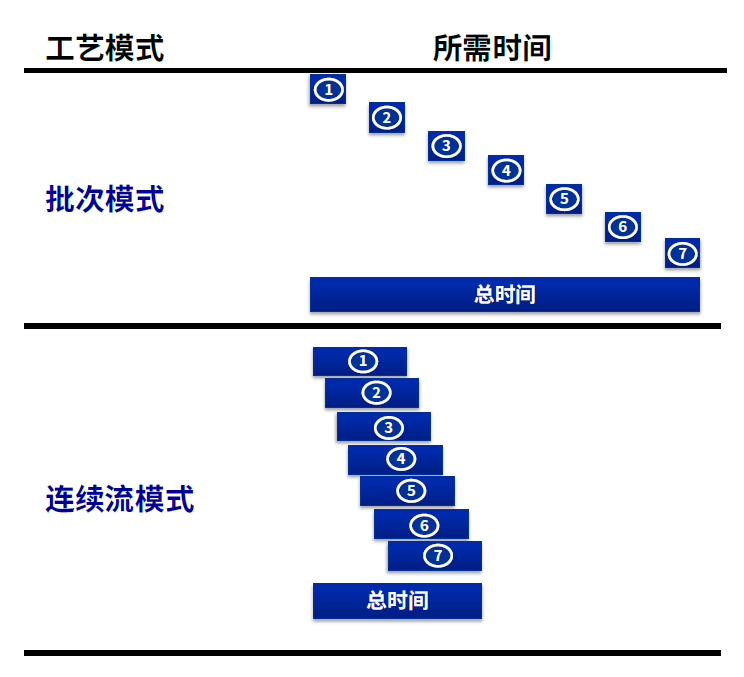
下游連續流工藝單元整合
未來,復宏漢霖也將繼續進行連續流生產技術的升級開發,希望通過持續的工藝創新不斷地提高產品質量,降低生產成本,逐步向生物葯生產的全自動化邁進,實現為全球患者提供質高價優生物葯的企業願景。
