2019年8月6號,漢利康®淋巴瘤科普公益團隊來到公益行程第五站——重慶市石柱縣。此次公益之行成功邀請到多位專家同行,上海血液學研究所常務副所長趙維蒞教授、陸軍軍醫大學新橋醫院血液病醫學中心主任張曦教授等淋巴瘤血液疾病領域的專家集聚一堂,開展疾病交流座談會、鄉村醫生培訓等公益活動,共同促進當地淋巴瘤等血液疾病學科的發展和規範化診療水平的提高。

石柱縣衛健委譚光榮主任、石柱縣人民醫院杜元洪書記、石柱縣人民醫院腫瘤科冉廣漢主任等對遠道而來的公益團隊一行表示了真摯的歡迎和感謝。石柱縣是重慶康養藝術的成功範例,今年4月15號,習總書記赴重慶考察調研,蒞臨石柱縣實地了解脫貧攻堅工作進展和解決「兩不愁三保障」突出問題情況。石柱縣多位領導指出:漢利康®淋巴瘤科普公益行正是對「兩不愁三保障」扶貧工作指示的貫徹落實,石柱縣將格外珍惜這次機會,為石柱縣腫瘤治療的發展奠定一個良好的基礎。

張曦教授表示:「漢利康®淋巴瘤科普公益行是一個落地到實處、對百姓有真正意義的公益項目,它非常符合中國的國情。復宏漢霖是國內很有責任的一家企業,他們關注整個扶貧活動。作為一名醫生來說,我很高興有機會加入到這個項目中來,貢獻自己的一份力量。相信在多方力量的共同推進下,這個項目將持續的開展下去,辦的越來越好。」

趙維蒞教授也提出了自己的一些思考:「作為年輕的學科帶頭人,我們可能能夠將一些東西做得很好,但是怎麼將自己的成績轉化,把在大醫院所取得的一些成就讓所有的醫院都能夠共享?我覺得這是一個重要的努力方向。我們做公益活動不僅僅出於一個醫生的熱情和責任,更應該把它做成一個事業,做成一個能夠長期持續的工作,這也需要民族企業、醫生、地方政府的共同努力,期待我們能夠攜手通力一起將這件事做好。」
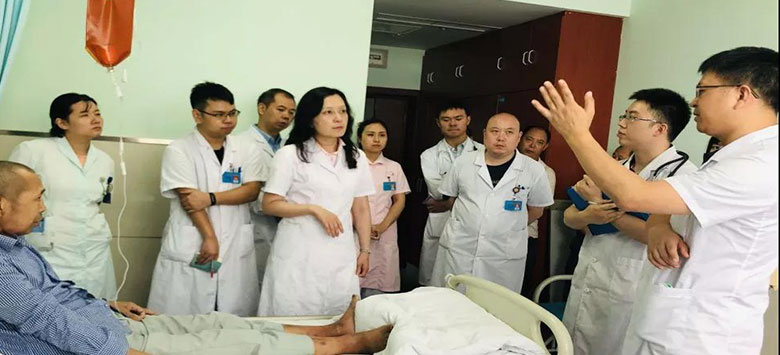
座談結束後,趙維蒞教授、張曦教授一行前往科室病房進行帶教查房。病房中,幾位專家針對患者們的病情進行了詳細的詢問,結合病例與現場就診結果及與科室醫生展開深入溝通交流,對患者們的治療方案提出了更為詳細的建議,也為年輕的科室醫生起到了良好的示範帶頭作用。

與此同時,陸軍軍醫大學新橋醫院血液病醫學中心副主任、淋巴腫瘤科主任劉耀教授、重慶醫科大學附屬第二醫院血液內科副主任鄧建川教授為當地的鄉村醫生帶來了專業知識培訓,圍繞「如何提高血液病的診療水平」進行了知識普及與病例分享,從血常規報告的解讀出發,提煉總結了多個真實病例中的常見狀況,實用而有效。


重慶市腫瘤醫院惡性淋巴瘤首席專家項穎教授前往門診部為當地血液病病患者進行義診,現場圍滿了聞訊趕來早早排隊等候的當地及周邊血液病患者。經過仔細的詢問與診斷,項教授依據患者病情提出切實的用藥改善方案及就醫指導,消除了患者對自身狀況很多不必要的擔憂。患者們得到專家的指點解答後,都滿懷感激不斷道謝,看到了儘快康復的希望。
公益團隊一行到達石柱縣當日,恰逢中國傳統的七夕節。愛與奉獻,讓這個團聚的節日變得更有意義!
漢利康®淋巴瘤科普公益行,我們一直在路上,敬請期待前方更多報道!
關於漢利康®淋巴瘤科普公益行
以惠及更多淋巴血液腫瘤患者為責任,為提高全國各地區對淋巴瘤疾病的防治、診斷及治療水平,復宏漢霖與江蘇復星醫藥銷售有限公司依託復星基金會鄉村醫生健康扶貧項目平台,於2019年1月正式啟動漢利康®淋巴瘤科普公益行項目。該項目從省會城市學術宣講為起點,下沉到當地省份的國家級貧困縣,專家醫療團隊對當地村醫、鄉鎮醫院醫生做淋巴瘤疾病的防治、診斷及治療方法的公益培訓,以提升當地對該疾病的認知及診療水平。
關於石柱縣
石柱土家族自治縣位於長江上游地區、重慶市東部、三峽庫區腹心,是集少數民族自治縣、三峽庫區淹沒縣、國家扶貧工作重點縣於一體的特殊縣份。
石柱縣東接湖北利川市,南連重慶彭水縣,西南臨重慶豐都縣,西北界重慶忠縣,北與重慶萬州區接壤。至2018年,石柱縣幅員面積3012平方公里,轄3個街道、17個鎮、13個鄉。戶籍人口為54.77萬人,常住人口為37.91萬人,有土家族、漢族、苗族、獨龍族等29個民族。
石柱縣為全國水土保持生態環境建設示範縣,獲得過「中國民間文化藝術之鄉」、「國家農業標準化辣椒生產示範區」等榮譽稱號。
關於復宏漢霖
復宏漢霖是一家中國領先的生物製藥公司,致力於為全球患者提供質高價優的創新生物葯。自2010年成立以來,公司在中國上海、台北和美國加州均設有研發中心,已經建立並持續拓展全面的生物類似葯及生物創新葯產品管線,產品覆蓋腫瘤、自身免疫性疾病等領域。
截至目前,復宏漢霖已有1個產品成功上市,2個產品獲得新葯上市申請受理,13個產品、6個聯合治療方案在全球範圍內開展20多項臨床試驗。其中,公司首款重磅產品漢利康®(利妥昔單抗注射液)於2019年2月獲國家葯監局新葯上市註冊批准,成為中國首個獲批上市的生物類似葯。HLX03(阿達木單抗注射液)與HLX02(注射用曲妥珠單抗)已獲國家葯監局新葯上市申請受理,現已納入優先審評程序。HLX02相繼在中國大陸、烏克蘭、歐盟波蘭和菲律賓全面啟動國際多中心3期臨床試驗,成為國內首個開展國際多中心3期臨床研究的生物類似葯,並於2019年6月獲歐洲藥品管理局上市申請受理。
