近日,復宏漢霖(2696.HK)宣佈,公司已在美國啟動一項針對創新抗PD-L1 抗體偶聯藥物(ADC)HLX43用於晚期或轉移性鱗狀非小細胞肺癌(sqNSCLC)的 II/III期國際多中心臨床研究(HLX43-NSCLC302)。該研究計劃於完成II期部分後,與FDA溝通並啟動後續的III期研究階段,有望成為HLX43首個、同時也是其在肺癌領域的關鍵註冊臨床研究,為既往標準治療失敗後的sqNSCLC患者這一難治群體帶來新的治療選擇。
肺癌是全球發病率和死亡率最高的癌症,2022年全球約有超過248萬新發肺癌病例 1。其中,非小細胞肺癌(NSCLC)是最常見的肺癌類型(約85%),可分為鱗狀細胞癌(約30%)、肺腺癌(約50%)等,且鱗狀NSCLC通常預後更差2。儘管以抗PD-1/L1單抗為代表的免疫檢查點抑制劑聯合化療顯著改善了晚期或轉移性鱗狀NSCLC患者的生存率。但在病情進展的2線或以上的後線人群治療上,療效優異的產品較少,主要依賴於多西他賽為基礎的化療方案,存在較大的未被滿足的臨床需求3-4。近年來,抗體偶聯藥物(ADC)在腫瘤治療中已展現出卓越的臨床療效,並在後線鱗狀NSCLC的臨床探索中顯示了積極信號5-6。同時,抗EGFR單抗聯合化療在鱗狀NSCLC治療中取得一定進展7-9,但療效多集中於EGFR高表達人群。抗EGFR單抗聯合新型治療方案在EGFR低表達患者中的療效亟待進一步探索。
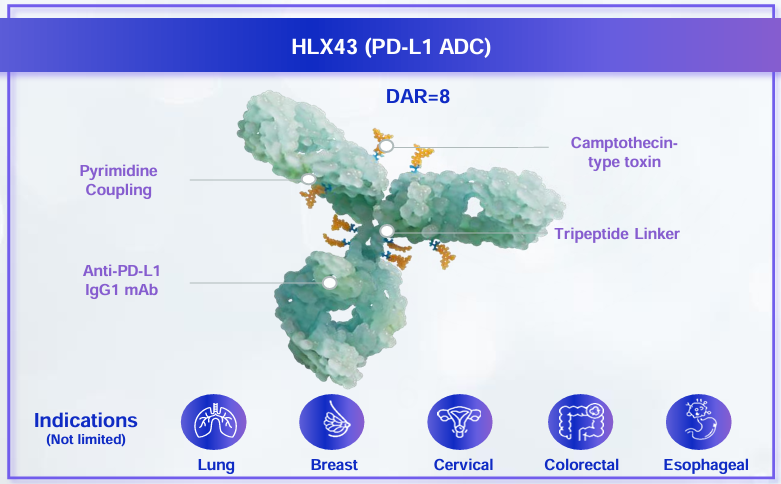
HLX43是一款潛在同類最優的廣譜抗腫瘤PD-L1 ADC,兼具免疫檢查點阻斷與載荷細胞毒性的雙重作用機制。目前,HLX43在NSCLC等實體瘤中展現出「高效、低毒」的初步臨床療效。根據2025 WCLC更新數據發佈,在鱗狀NSCLC的後線治療中,HLX43已展現出初步的臨床優勢,接受2mg/kg劑量HLX43治療的患者客觀緩解率(ORR)達40.0%,疾病控制率(DCR)為73.3%。此外,針對多西他賽治療失敗的三線及後線NSCLC患者,HLX43的ORR仍達到30.0%,DCR為80%。HLX07是復宏漢霖自主開發的創新型抗EGFR的單抗,相比西妥昔單抗該產品具備更低的免疫原性和更好的靶點親和力。根據2025 WCLC最新數據發佈,HLX07聯合斯魯利單抗及化療在EGFR高表達sqNSCLC患者一線治療中展現出顯著的抗腫瘤活性和持久療效,在中位隨訪18.6個月時實現了約70%的客觀緩解率(ORR)和超過90%的疾病控制率(DCR),且在高劑量組的中位無進展生存期(PFS)達到17.4個月。因此,HLX43有望協同抗EGFR單抗HLX07,發揮出較HLX43單藥及抗EGFR單抗聯合化療更高的治療潛力,進一步提升鱗狀NSCLC等晚期實體瘤患者的治療獲益。
目前,復宏漢霖正全力推進HLX43的臨床開發進程,在全球入組超過700例患者。其中NSCLC患者佔比超過60%(400例),包括一項針對NSCLC的國際多中心II期臨床研究(HLX43-NSCLC201)正在中、美、日、澳等地同步開展。此外,公司已累計開展十餘項HLX43單藥或聯合其他產品的臨床研究,廣泛覆蓋宮頸癌(CC)、食管鱗癌(ESCC)、頭頸鱗癌(HNSCC)、鼻咽癌(NPC)、結直腸癌(mCRC)、胃癌/胃食管交界部(G/GEJ)癌、胰腺導管腺癌(PDAC)、乳腺癌(BC)等,持續探索和挖掘HLX43在實體瘤中的廣譜治療潛力,其在CC、ESCC、NPC、HNSCC等腫瘤中的概念驗證數據已在/將在ESMO Asia、ASCO GI、ASCO、ESMO等大會上陸續讀出。單藥之外,基於HLX43展現出的IO療效,公司積極探索HLX43與其他多元分子如公司自研創新抗EGFR單抗HLX07、H藥 漢斯狀®(斯魯利單抗,抗PD-1單抗)的聯合治療潛力,不斷挖掘和最大化該產品在臨床中的應用價值。
未來,復宏漢霖將持續聚焦患者未滿足的臨床需求,立足於HLX43等核心創新管線,不斷放大產品的差異化治療潛力,加速推動更大臨床價值的釋放,為全球患者帶來更具突破療效的治療方案。
關於HLX43-NSCLC302
本研究為一項隨機、開放標籤、國際多中心 II/III 期臨床研究,旨在評估HLX43(抗PD‑L1的ADC)單藥或HLX43聯合 HLX07(重組抗EGFR人源化單克隆抗體注射液),相較於多西他賽,在既往治療失敗的晚期/轉移性鱗狀非小細胞肺癌(NSCLC)患者中的 療效和安全性。
該研究包括兩個階段。第一階段為一項開放標籤、隨機、多中心的II期研究,符合入選標準的受試者將按照 1:1:1的比例隨機分配至A組(HLX43 單藥),B組(HLX43 聯合 HLX07)或C組(多西他賽)。第二階段為一項開放標籤、隨機、多中心的III期研究,將根據第一階段結果選定 HLX43單藥或HLX43聯合HLX07作為試驗組方案。計劃入組約566例受試者,並按照1:1的比例隨機分配至試驗組(HLX43單藥或HLX43聯合HLX07)或對照組(多西他賽)。本研究研究主要目的是評估HLX43單藥或HLX43聯合HLX07對比多西他賽在經一線治療失敗的晚期鱗狀NSCLC患者中的臨床療效,採用總生存期(OS)和無進展生存期(PFS)作為雙主要終點。次要目的包括評價HLX43單藥或HLX43聯合HLX07的安全性、HLX43和HLX07的藥代動力學(PK)特徵、免疫原性,以及探索潛在的預測性或耐藥性生物標誌物。
【參考文獻】
1.Bray F, Laversanne M, Sung H, et al. Global cancer statistics 2022: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2024;74(3):229-263.
2.Wang, Y., et al. Immunotherapy for advanced-stage squamous cell lung cancer: the state of the art and outstanding questions. Nat Rev Clin Oncol 22, 200–214 (2025).
3.中國臨床腫瘤學會 中國臨床腫瘤學會(CSCO). (2024)非小細胞肺癌診療指南
4.NCCN Guidelines Version 3. 2025, Non-Small Cell Lung Cancer.
5.Ahn MJ, et al. TROPION-Lung01 Trial Investigators. Datopotamab Deruxtecan Versus Docetaxel for Previously Treated Advanced or Metastatic Non-Small Cell Lung Cancer: The Randomized, Open-Label Phase III TROPION-Lung01 Study. J Clin Oncol. 2025 Jan 20;43(3):260-272.
6.Paz-Ares LG, et al. Sacituzumab Govitecan Versus Docetaxel for Previously Treated Advanced or Metastatic Non-Small Cell Lung Cancer: The Randomized, Open-Label Phase III EVOKE-01 Study. J Clin Oncol. 2024 Aug 20;42(24):2860-2872.
7.Pirker R, et al. EGFR expression as a predictor of survival for first-line chemotherapy plus cetuximab in patients with advanced non-small-cell lung cancer: analysis of data from the phase 3 FLEX study. Lancet Oncol. 2012 Jan;13(1):33-42.8.
8.Thatcher N, et al. Necitumumab plus gemcitabine and cisplatin versus gemcitabine and cisplatin alone as first-line therapy in patients with stage IV squamous non-small-cell lung cancer (SQUIRE): an open-label, randomised, controlled phase 3 trial. Lancet Oncol. 2015 Jul;16(7):763-74.
9.Becotatug (JMT101, Beco) combined with docetaxel (albumin-bound, HB1801) for the treatment of patients (pts) with locally advanced squamous cell non-small cell lung cancer (sqNSCLC): A randomized control phase II study (BATTLE study). ESMO Asia 2025|2025-12-05.
