2022年8月26日,復宏漢霖(2696.HK)宣佈,公司自主開發的HLX60(創新型抗GARP單抗)聯合公司自主開發的PD-1抑制劑H藥 漢斯狀®(斯魯利單抗)已於澳大利亞獲得相關人類研究倫理委員會的批准並通過澳大利亞藥品管理局(Therapeutic Goods Administration,TGA)的臨床試驗備案,被批准開展I期臨床研究,擬用於晚期或轉移性實體瘤的治療。目前,全球範圍內尚無GARP抑制劑獲批上市。
近年來,免疫檢查點療法為腫瘤治療提供了新的途徑。目前研究和應用最廣泛的免疫檢查點抑制劑包括CTLA-4(細胞毒性T淋巴細胞相關抗原-4)、PD-1(程序性細胞死亡蛋白1)及其配體PD-L1(程序性細胞死亡配體1)的抑制劑等。PD-1/PD-L1信號通路在腫瘤免疫中具有重要作用,PD-1和PD-L1抑制劑目前已被批准用於黑色素瘤、非小細胞肺癌、肝細胞癌、經典霍奇金淋巴瘤等。儘管如此,研究發現只有30-40%的患者可從免疫檢查點療法治療中受益,且仍將面臨腫瘤復發或進展的可能,此外,一些特定癌種亦對免疫檢查點療法缺少響應[1-2]。基於未滿足的巨大臨床需求,更多新的療法亟需被開發。
轉化生長因子-β(TGF-β)是一種多效細胞因子,在多種組織中均有表達,有TGF-β1、TGF-β2、TGF-β3三個主要亞型,其中TGF-β1在細胞增殖、發育、凋亡、纖維化、血管生成、傷口癒合、癌症免疫等生物學過程的許多方面都發揮着重要作用[3-5]。糖蛋白 A 重複優勢蛋白(glycoprotein-A repetitions predominant,GARP)是潛伏轉化生長因子β1(LTGF-β1)的對接受體,其主要在活化的調節性T細胞(Tregs)和血小板上表達[6],在腫瘤微環境(TME)中富集並激活TGF-β1,從而抑制抗腫瘤免疫應答,促進腫瘤細胞生長、增殖和侵襲[7-8]。
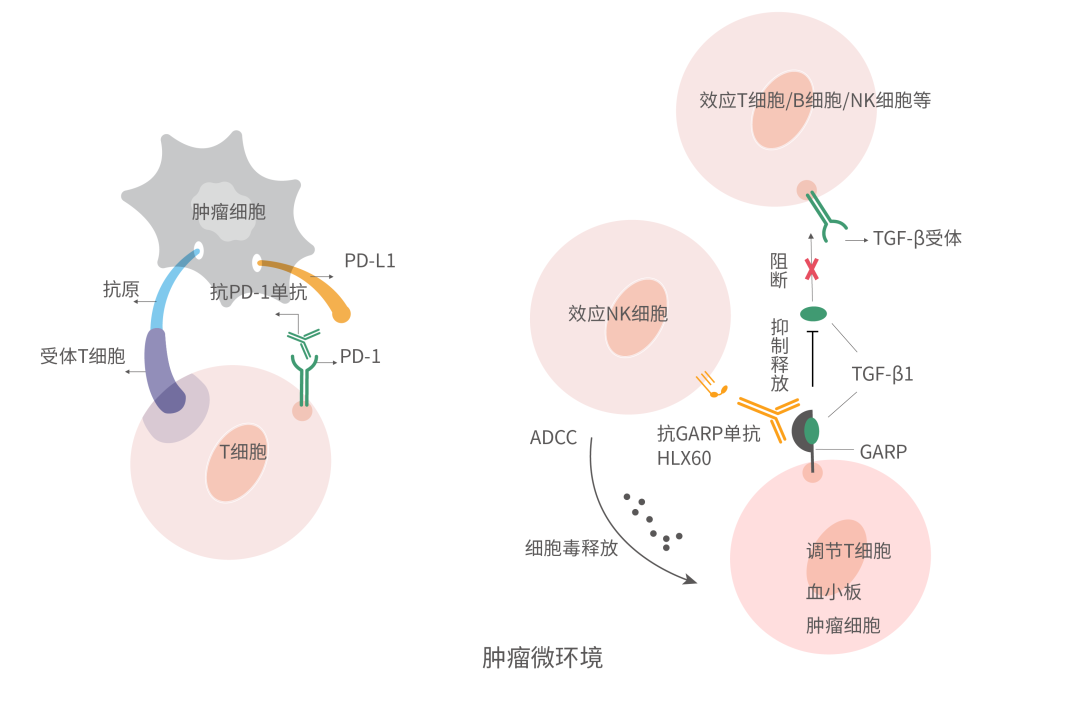
HLX60為復宏漢霖自主研發的靶向GARP的創新型單抗,其可通過特異性結合GARP,阻斷GARP介導的TGF-β1的釋放,逆轉TME中的免疫抑制效應,提高抗腫瘤免疫應答。此外,HLX60可以通過抗體依賴細胞介導的細胞毒作用(ADCC)清除GARP陽性腫瘤細胞和Tregs等免疫抑制性細胞,從而發揮抗腫瘤作用。臨床前研究結果顯示,HLX60與漢斯狀®聯用的抗腫瘤效果明顯優於漢斯狀®或HLX60單藥治療效果,具有良好的耐受性和安全性,充分體現出雙免疫療法的協同抗腫瘤效應。
復宏漢霖從臨床需求出發,目前在PD-1/L1、CTLA-4、LAG-3等免疫檢查點全面佈局,為免疫聯合治療的探索創造更多可能。同時,公司充分運用自有管線覆蓋腫瘤特異性靶點、抗血管生成靶點和腫瘤免疫靶點等多個類別的特點,助力H藥與自有單抗產品、化療等治療手段開展聯合治療,已廣泛覆蓋肺癌、食管癌、頭頸鱗癌和胃癌等適應症,有助於充分挖掘免疫療法的治療潛力,為全球患者帶去高品質、可負擔的創新治療方案。
關於H藥 漢斯狀®
H藥 漢斯狀®為重組人源化抗PD-1單抗注射液(通用名:斯魯利單抗注射液),是復宏漢霖首個自主研發的創新型單抗,目前1項適應症獲批上市,3項適應症上市申請獲受理,11項臨床試驗同步在全球開展。
2022年3月,H藥正式獲批用於治療微衛星高度不穩定(MSI-H)實體瘤。圍繞H藥,復宏漢霖積極推進其與公司其他產品的協同以及與創新療法的聯合,相繼獲得中國、美國、歐盟等國家及地區的臨床試驗許可,在全球同步開展11項腫瘤免疫聯合療法臨床試驗,廣泛覆蓋肺癌、食管癌、頭頸鱗癌和胃癌等適應症,全面覆蓋肺癌一線治療。截至目前,H藥已於中國、土耳其、波蘭、格魯吉亞等國家和地區累計入組超3100人,其中2項國際多中心臨床試驗入組高加索人種的比例超過30%,是擁有國際臨床數據較多的抗PD-1單抗之一。H藥聯合化療一線治療鱗狀非小細胞肺癌(sqNSCLC)、廣泛期小細胞肺癌(ES-SCLC)和食管鱗狀細胞癌(ESCC)的NDA已獲得NMPA受理,H藥有望成為全球首個一線治療SCLC的抗PD-1單抗。此外,該藥入選《2022 CSCO小細胞肺癌診療指南》作為ES-SCLC治療推薦,其治療小細胞肺癌(SCLC)也已獲得美國FDA孤兒藥資格認定。
參考文獻
[1] Kanjanapan Y, Day D, Wang L et al. Hyperprogressive disease in early-phase immunotherapy trials: Clinical predictors and association with immune-related toxicities. Cancer 2019; 125: 1341-1349.
[2] Chowdhury PS, Chamoto K, and Honjo T. Combination therapy strategies for improving PD-1 blockade efficacy: a new era in cancer immunotherapy. J Intern Med 283, 2017, 110-120.
[3] Gordon KJ, Blobe GC. Role of transforming growth factor-beta superfamily signaling pathways in human disease. Biochim Biophys Acta. 2008;1782(4):197–228.
[4] Kulkarni AB, Karlsson S. Transforming growth factor-beta 1 knockout mice. A mutation in one cytokine gene causes a dramatic inflammatory disease. Am J Pathol. 1993;143(1):3–9.
[5] Li MO, Wan YY, etc. Transforming growth factorbeta regulation of immune responses. Annu Rev Immunol. 2006; 24:99–146.
[6] Roubin R, Pizette S, Ollendorff V, Planche J, Birnbaum D and Delapeyriere O. Structure and developmental expression of mouse Garp, a gene encoding a new leucine rich repeat-containing protein. The International journal of developmental biology. 1996;40(3):545-555.
[7] Edwards JP, Thornton AM, Shevach EM. Release of active TGF-beta1 from the latent TGF-beta1/GARP complex on T regulatory cells is mediated by integrin beta8. J Immunol. 2014;193(6):2843–9.
[8] Stockis J, Lienart S, etc. Blocking immunosuppression by human Tregs in vivo with antibodies targeting integrin alphaVbeta8. Proc Natl Acad Sci U S A. 2017; https://doi.org/10.1073/pnas.1710680114.
