2023年6月6日,复宏汉霖(2693.HK)宣布公司自主研发的针对EGFR靶点的创新型生物药HLX07在局部晚期、不可切除或转移性食管鳞状细胞癌患者中II期研究(HLX07-ESCC201) 结果以海报形式入选ASCO年会。该研究由国家癌症中心/国家肿瘤临床医学研究中心/中国医学科学院北京协和医学院肿瘤医院黄镜教授牵头开展。
HLX07是复宏汉霖自主研发的针对EGFR靶点的创新型生物药。基于公司成熟的抗体工程改造平台,复宏汉霖在西妥昔单抗的基础上,通过将HLX07的Fab区人源化,同时使该产品聚糖含量降至最低,以具备更低的免疫原性和良好的靶点亲和力。复宏汉霖已就HLX07在中国、美国、欧盟、澳大利亚、日本等多个知识产权区获得专利,并在中国和美国获得临床试验许可。目前,公司围绕食管鳞癌、皮肤鳞癌等多个实体瘤适应症,正在积极开展HLX07单药或联合H药 汉斯状®(斯鲁利单抗)的II期临床探索。此次ASCO年会上发布的数据详情如下:
论文题目
HLX07单药或联合疗法在局部晚期、不可切除或转移性食管鳞状细胞癌患者中的Ⅱ期研究(摘要编号4029)
试验设计
此研究为一项开放标签、多中心的Ⅱ期研究。试验纳入年龄为18–75岁、经组织学或细胞学确认的局部晚期、不可切除/转移性食管鳞状细胞癌(ESCC)或食管腺鳞癌患者。既往未接受过全身抗肿瘤治疗的患者被分配至A组,给予HLX07 1000 mg(抗EGFR单克隆抗体)联合斯鲁利单抗200 mg(抗PD-1单克隆抗体)及化疗(5-FU 2400 mg/m2 + 顺铂50 mg/m2),每两周一次静脉输注。一线免疫联合化疗治疗失败或至少两种其他系统性抗肿瘤治疗失败的患者被分配至B组,并给予HLX07单药治疗(1000mg,每两周一次静脉输注)。试验的主要终点是由独立影像评估委员会和研究者根据RECIST v1.1评估的客观缓解率(ORR)和无进展生存期(PFS)。次要终点包括其他疗效指标、安全性、药代动力学特征、免疫原性和生物标志物探索。

结果
截至2023年2月4日,共49例患者入组至A组(n = 30)和B组(n = 19),中位年龄分别为64.5岁和59.0岁。A组26(86.7%)例患者和B组所有患者为男性。中位随访时间为2.9个月,本次报告的为初步疗效。
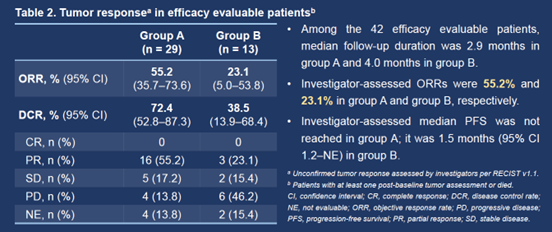
在42例可评估疗效的患者中(A组29例,B组13例),研究者评估的ORR分别为55.2%(95% CI 35.7–73.6%)和23.1%(95% CI 5.0–53.8%)。研究者评估的中位PFS在A组中未达到,在B组中为1.5个月(95% CI 1.2–不可评估)。
与HLX07相关的多数不良事件为一级及二级。A组16(53.3%)例和B组11(57.9%)例患者报告了特别关注不良事件,最常见的是皮疹(43.3%对比47.4%)和低镁血症(33.3%对比36.8%)。试验未报告与药物相关的死亡。
结论
研究显示,对于晚期食管鳞癌患者,HLX07具有良好的抗肿瘤活性和可控的安全性。
